近日����,福建醫(yī)科大學福州總醫(yī)院藥學科主任宋洪濤教授的研究團隊在二氧化錳納米材料的制備和化學光熱療法治療腫瘤方面取得了重要進展,相關研究成果“Photothermal MnO2 nanoparticles boost chemo-photothermal therapy-induced immunogenic cell death in tumor immunotherapy”已經(jīng)發(fā)表在醫(yī)學綜合期刊《International Journal of Pharmaceutics》(IF:6.51�����,一區(qū)Top期刊 )上��。

圖1 醫(yī)學綜合期刊《International Journal of Pharmaceutics》
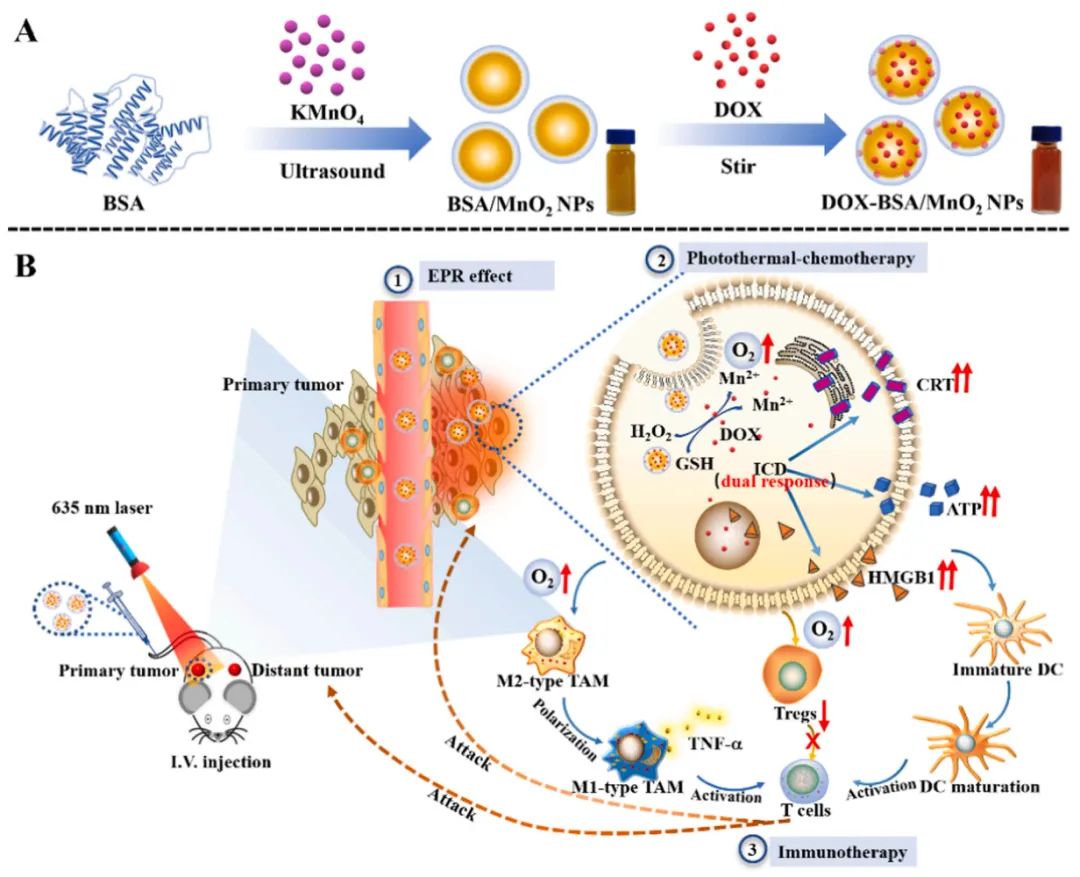
圖2 用納米材料DOX-BSA/MnO2 NPs誘導免疫治療腫瘤細胞的機理����,其介導的光熱療法可以抑制原發(fā)腫瘤和異位腫瘤的生長����,有效地改善免疫抑制微環(huán)境,以利于腫瘤的免疫治療
誘導原位自發(fā)性腫瘤細胞死亡(ICD)在癌癥預防和個性化免疫治療方面具有巨大的研究價值����。但是,ICD在腫瘤免疫治療中的有效性受到很大限制����,主要由于誘導效率低以及受到抑制免疫力的腫瘤微環(huán)境(TME)影響����。
為此�����,研究團隊開發(fā)了一種新的光熱療法誘導ICD的方法����,即在腫瘤免疫治療中使用負載阿霉素(DOX)的光熱MnO2納米顆粒���,以克服傳統(tǒng)ICD誘導劑的低效性。首先通過牛血清白蛋白直接還原KMnO4制備了具有良好水分散性和生物相容性的光熱牛血清白蛋白-MnO2 NP(BSA/MnO2 NPs)的納米材料���,然后將ICD誘導劑阿霉素裝載到MnO2 NPs上。
所制備的DOX-BSA/MnO2 NPs納米藥物在三陰性乳腺癌荷瘤小鼠模型中取得了顯著的體內(nèi)協(xié)同治療效果��,實現(xiàn)了高光熱轉(zhuǎn)換效率�、高效腫瘤靶向性、腫瘤微環(huán)境下阿霉素的釋放和氧含量調(diào)節(jié)作用����。
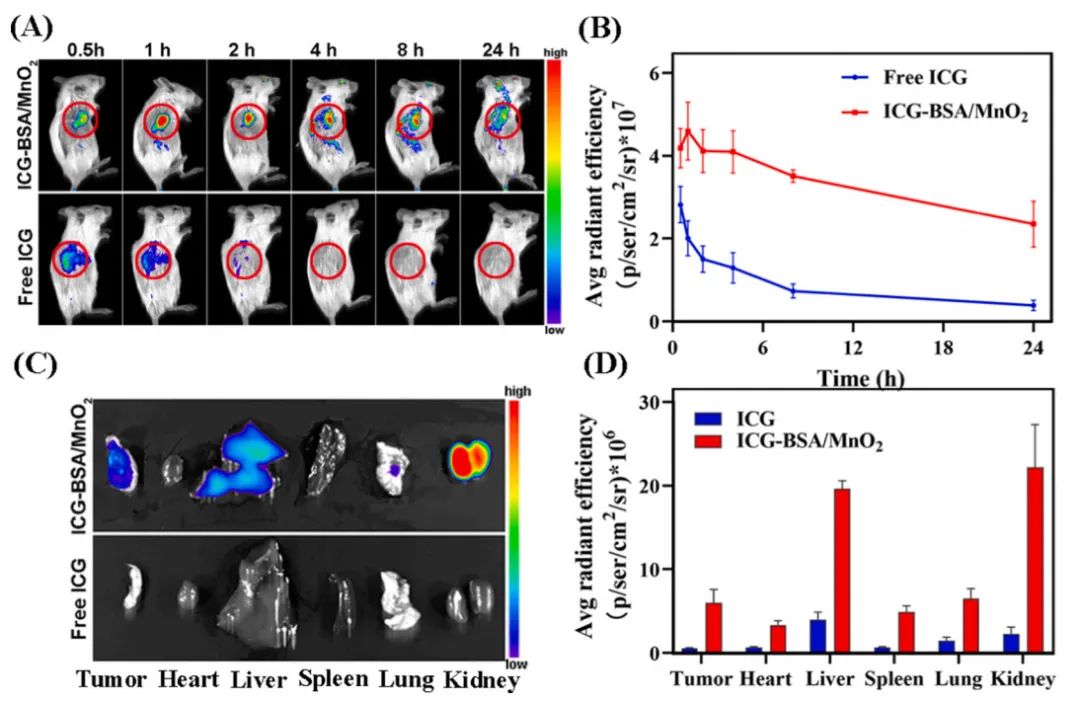
圖3 靜脈注射ICG標記的DOX-BSA/MnO2 NPs納米材料到BALB/c小鼠模型
此項研究指明了用光熱MnO2納米系統(tǒng)調(diào)節(jié)腫瘤微環(huán)境以增強腫瘤免疫治療效果有巨大應用前景�����。

文章中小鼠熒光圖像結果使用博鷺騰AniView多模式動物活體成像系統(tǒng)拍攝����。
論文鏈接https://doi.org/10.1016/j.ijpharm.2022.121578